Иметь представление о том, что такое правила «хорошей» (надлежащей) лабораторной практики (Good Laboratory Practice) или правила GLP полезно для производителя косметических средств по двум причинам: для контроля качества закупаемого косметического сырья и для подтверждения эффективности производимых косметических средств.
Что же такое принципы GLP, и почему они были созданы? В семидесятые годы прошлого века Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration (FDA)), функцией которого является контроль за безопасностью продуктов и лекарств в США, анализируя представленную на рассмотрение документацию, выявило несколько случаев мошенничества. Несколькими фармацевтическими компаниями в FDA были предоставлены недостоверные данные токсикологических исследований, полученные в различных научно-исследовательских лабораториях. В этих лабораториях либо откровенно фальсифицировали результаты токсикологических испытаний безопасности различных химических веществ, вовсе не проводя их, либо проведенные исследования были такого низкого качества, что при их аудите даже не удавалось понять, какая именно работа была проделана (1). Самые значимые среди обнаруженных недостатков были:
- недостаточно подробно составленный план исследования;
- недостоверные методики постановки эксперимента, например, неправильная калибровка оборудования, неправильная последовательность опытов, неправильно оформленная документация;
- неточная и неполная регистрация данных;
- ошибки в научном отчете (выводы не соответствуют полученным экспериментальным данным).
Эти проблемы привели к тому, что в 1976 году FDA опубликовало первоначальный вариант правил GLP, а окончательное постановление было принято в июне 1979 года (21 CFR 58).
Агентство по охране окружающей среды (EPA) также столкнулось с проблемой недобросовестно проведенных исследований, и выпустило проекты своих собственных правил GLP в 1979 и в 1980 годах, а окончательный вариант правил был опубликован в двух отдельных частях (40 CFR 160 и 40 CFR 792) в 1983 году (2).
Принятие принципов GLP в странах ОЭСР
Организация экономического сотрудничества и развития (сокр. ОЭСР, англ. Organisation for Economic Co-operation and Development, OECD) – это международная экономическая организация развитых стран, признающих принципы представительной демократии и свободной рыночной экономики. Страны-члены ОЭСР производят две трети товаров и услуг в мире.
Правила GLP для доклинических исследований, опубликованные Food and Drug Administration в США, послужили основой для работы Группы экспертов по разработке Принципов GLP в странах ОЭСР (3). Эти принципы были официально рекомендованы Советом стран для использования в странах-членах ОЭСР в 1981 году. Они стали неотъемлемой частью решения Совета по взаимному признанию данных (Council Decision on Mutual Acceptance of Data (MAD)) в оценке химических веществ, которое гласит, что «данные, полученные в результате тестирования химических веществ в странах-членах ОЭСР и в соответствии с руководящими принципами ОЭСР (OECD Test Guidelines) и принципами надлежащей лабораторной практики (OECD Principles of Good Laboratory Practice), должны быть приняты в других странах-членах ОЭСР в целях оценки и других целях, связанных с защитой человека и окружающей среды» [C(81)30(Final)].
В соответствии с MAD – соглашением о взаимном признании результатов экспериментальной оценки химических веществ, полученных в соответствии с Рекомендациями о соблюдении принципов надлежащей лабораторной практики [C (89) 87 (Final)] Совет решил, что страны-члены ОЭСР должны создать национальные процедуры мониторинга соблюдения Принципов GLP, основанные на лабораторных проверках и ревизиях исследований.
Важно подчеркнуть, что соглашение о взаимном признании результатов испытаний действительно только в странах-членах ОЭСР и является удобным инструментом, упрощающим обращение в этих странах химических веществ.
Соблюдение правил GLP членами ОЭСР дает следующие возможности:
- Многостороннего соглашения с другими странами ОЭСР о принятии данных исследований химических веществ, проведенных в соответствии с принципами GLP ОЭСР;
- Выполнения научных исследований в соответствии с единым стандартом качества GLP ОЭСР;
- Позволяет избежать дублирования работы и уменьшить финансовые расходы со стороны правительственных организаций, промышленности и испытательных органов;
- Содействие обмену информацией и предотвращение возникновения нетарифных барьеров в торговле.
Механизм многостороннего соглашения схематично показан на Рис.1.
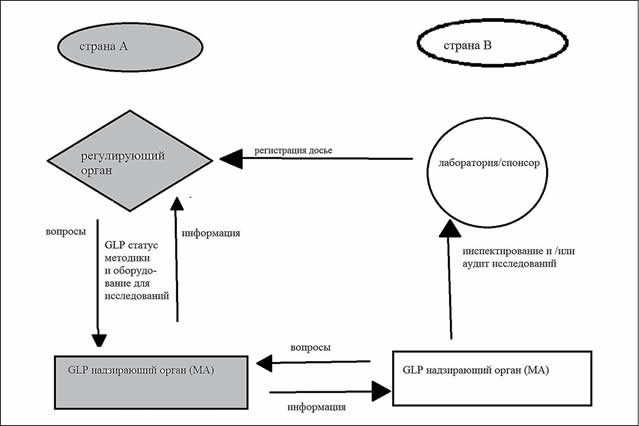
Рис. 1. Механизм многостороннего соглашения, основанного на принятии принципов OECD GLP
Возможны три варианта взаимодействия стран в связи со взаимным принятием результатов экспериментальных исследований:
- Страны А и В являются странами-членами ОЭСР: в соответствии с MAD, необработанные экспериментальные данные тестирования объектов, полученные в стране В, принимаются страной А и наоборот (в том числе, и в других странах-членах ОЭСР).
- Страна А является, а страна В не является страной-членом ОЭСР. Исходные данные испытаний объектов, полученные в стране В, согласно двухстороннему соглашению, могут быть приняты только в стране А, если специальный инспектирующий орган (Monitoring Authority, MA) проведет мониторинг, проверяя, были ли представленные данные получены в соответствии с принципами GLP ОЭСР. Тем не менее, даже если эти данные принимаются одной страной-членом ОЭСР, это не означает, что они будут приняты в других странах-членах ОЭСР автоматически. Существует потенциальный риск, что данные, полученные в лабораториях страны В для испытуемых объектов, будут проверяться в странах-членах ОЭСР всякий раз, когда они будут представлены заинтересованной стороной (лабораторией или спонсором исследований) на рассмотрение регулирующих органов страны-члена ОЭСР.
- Страны А и В не являются членами ОЭСР: результаты исследований признаются этими двумя странами на основе двустороннего соглашения. Данные исследований, выполненных в обеих странах, не принимаются странами-членами ОЭСР.
В настоящее время опытные эксперты GLP организуют учебные курсы по применению принципов ОЭСР GLP в странах, заинтересованных в развитии этой системы качества, в группах, не превышающих 20 человек. Это может быть общий курс, посвященный основным понятиям и принципам ОЭСР GLP и объяснению возможных трудностей, связанных с применением GLP ОЭСР. Кроме того, этот курс обеспечивает разнообразие упражнений и тематических исследований. В результате такого учебного курса создается план внедрения GLP и проходит его осуществление. Учебный курс следующего уровня посвящен оценке прогресса в разработке и реализации принципов ОЭСР GLP в соответствии с принятым планом. Этот учебный курс должен быть организован в течение одного года после первого учебного курса, в зависимости от прогресса в реализации принципов ОЭСР GLP. Кроме того, организуется экспертная помощь на этапе подготовки рабочей программы, внедрения, составления отчетности и осуществляются действия для коррекции недостатков, выявленных в ходе проверок.
Ссылки
- Schneider, K (1983(Spring)). «Faking it: The case against Industrial Bio-Test Laboratories” Amicus Journal (Natural Resources Defence Council): 14–26.
- Staff, World Health Organization (2009) Handbook: Good Laboratory Practice (GLP) «OECD Principles of Good Laboratory Practice (as revised in 1997)». OECD Environmental Health and Safety Publications (OECD) 1. 1998.
- Материал подготовлен на основе статьи Mr. Hedwig Beernaert «Application and Importance of the Principles of OECD Good Laboratory Practice (GLP)», опубликованной на http://chemlinked.com/expert-article/application-and-importance-principles-oecd-good-laboratory-practice-glp#sthash.tuVHf6ga.dpuf


