| Т.А. Гирш, эксперт-аудитор ВНИИС по сертификации систем менеджмента и GMP, В.В. Устинов, главный эксперт-аудитор ВНИИС по сертификации систем менеджмента и GMP |
В январе 2012 г. вступил в действие технический регламент Таможенного союза ТР ТС 009/2011«О безопасности парфюмерно-косметической продукции». Прошло 3 года и можно попытаться подвести какие-то итоги. Предварительный вывод, который напрашивается: ничего практически не изменилось. Откуда такой пессимизм? Поясним. Регламент – документ (имеющий статус закона!), который должен сподвигнуть производителей на улучшения как в части требований к безопасности конечной продукции, так и в части создания условий обеспечения этой безопасности на стадии производства. Второе особенно важно, поскольку в 21 веке в России изменилась сама парадигма обеспечения безопасности продукции, которая стала похожа на европейскую: произошел переход от тотального контроля продукции (отбор образцов от каждой партии, испытания в аккредитованной лаборатории) к созданию и контролю условий обеспечения качества и безопасности на стадии производства.
В этой связи характерен пример пищевой отрасли. После введения с 15.02.15 г. в действие аналогичного регламента ТР ТС 021 «О безопасности пищевой продукции» производители атаковали институты Росстандарта и консалтинговые компании всех калибров и достоинств с просьбами разъяснить требования к производству и помочь их внедрить. Требования были не самые простые: они базировались на международных документах комиссии Codex Alimentarius, включая помимо анализа рисков также применение надлежащей производственной практики (GMP).
С регламентом ТР ТС 009 этого не произошло, ажиотажа не было. Почему? Ответ на этот вопрос можно получить, взглянув на рисунок и табл. 1.
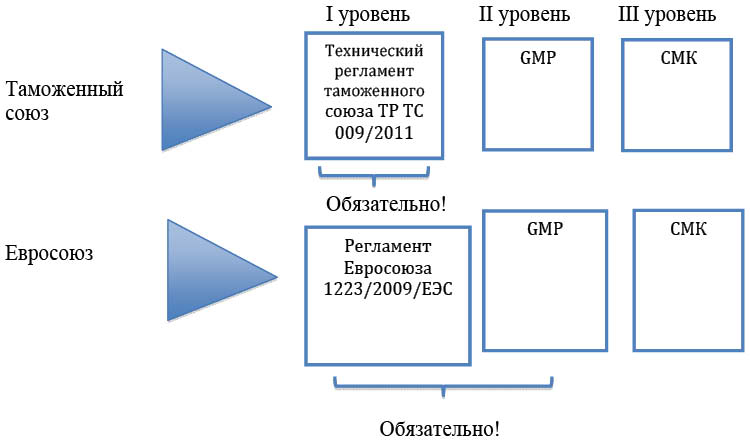
Рисунок 1. Обеспечение безопасности парфюмерно-косметической продукции при изготовлении
На рис. 1 представлено сравнение двух подходов к обеспечению качества и безопасности на стадии производства: Таможенного союза и Евросоюза. Как видим, структура регулирующих документов похожа.
Первый уровень: Регламенты. Наш ТР ТС 009 имеет раздел 7, где приведены детализированные в той или иной степени требования к условиям производства. Европейский регламент 1223/2009/ЕЕС содержит в разделе 8 простую ссылку на обязательность (!) для производства GMP.
Второй уровень:GMP. Требования одинаковые у нас и у них, поскольку в Таможенном союзе используется стандарт ГОСТ ISO 22716–2007, идентичный европейскому ISO 22716–2007.
Третий уровень: СМК. И у нас и у них базой является стандарт ИСО 9001.
Как видно из рисунка, с точки зрения технического регулирования европейский подход более «продвинутый», т.к. распространяет обязательность и на документ второго уровня: GMP. Но быть может требования к производству из раздела 7 нашего регламента ТР ТС 009 не слабее требований ISO 22716–2007 ( GMP)? Отнюдь. Из 17 разделов стандарта GMP, содержащих требования, только половина с той или иной степенью детализации увязаны с ТР ТС 009. При этом, требования ни одного из разделов международного стандарта GMP не вошли полностью в регламент Таможенного союза. Вот и ответ на вопрос: почему промышленность «спит спокойно» после введения в действие ТР ТС 009.
Ситуация сейчас похожа на ту, которая наблюдалась в российской пищевой промышленности лет 15 назад, когда ХАССП и GMP вовсю внедрялись в Европе, а разработанный российский стандарт на эту тему применялся очень немногими компаниями, которые в конечном итоге и получили ряд серьезных преимуществ:
- практически исчезли рекламации по безопасности и серьезные претензии контролирующих органов (т.к. «слабые» места выявили и устранили на стадии производства);
- аудиты второй стороной для размещения производств солидными заказчиками под собственной торговой маркой (СТМ) проходили без каких-либо значительных проблем.
Эти же преимущества, не дожидаясь обязательности внедрения GMP, (как это, кстати, произошло в фармацевтической отрасли в 2014 г.) могут получить и производители парфюмерно-косметической продукции (в первую очередь речь, конечно, идет об аудитах второй стороной для размещения заказов на производство продукции от производителей известных зарубежных брэндов). И получить уже сейчас, несмотря на кризис, поскольку в отличие от пищевых и фармацевтических стандартов внедрение GMP для производств парфюмерно-косметической продукции скорее всего не будет стоить огромных денег.
Взгляните на таблицу. В ней обобщены наблюдения авторов, которым по роду деятельности приходилось заниматься внедрением или оценкой GMP и систем менеджмента качества (СМК) на предприятиях отрасли («Красная линия», «Русская косметика», «РусХимХолдинг», «Фрэнчи продактс» и др.). В таблице указаны наиболее часто встречающиеся проблемы и приведена наша экспертная оценка усилий (затрат) по их решению при разработке и внедрении GMP (или систем качества, разрабатываемых с учетом требований GMP).
Таблица 1. Типичные проблемы и оценка возможных затрат при внедрении GMP
|
Объект требований по ISO 22716 |
Типичная проблема |
Дополнительные затраты на решение проблемы |
|---|---|---|
|
Персонал |
организация обучения |
минимальные |
|
Помещения |
планировки, вентиляция |
как правило, требуются |
|
Оборудование |
использование резервных систем |
как правило, не требуются |
|
Сырье и упаковочные материалы |
условия хранения и идентификация |
не требуются или минимальные |
|
Производство |
наличие документации |
не требуются |
|
Готовая продукция |
— |
— |
|
Лаборатория |
— |
— |
|
Обращение с несоответствующей продукцией |
документация по повторно перерабатываемой продукции |
не требуются |
|
Отходы |
— |
— |
|
Субподрядные договоры |
аудиты субподрядчиков |
не требуются |
|
Отклонения |
— |
— |
|
Рекламации и отзыв |
моделированные отзывы продукции |
не требуются |
|
Контроль изменений |
— |
— |
|
Внутренний аудит |
организация внутренних аудитов |
не требуются или минимальные |
|
Документация |
управление документацией |
не требуются |
Как видим, определенные затраты скорее всего возможны при обустройстве подходящей производственной зоны (в части планировок помещений, систем водоподготовки и вентиляции). При этом следует сразу оговориться, что уровень затрат существенно зависит от:
- характеристик продукции (т.е. требуемого класса чистоты помещений);
- возраста и изначальной пригодности инфраструктуры (имеются ввиду арендованные площади или специально построенные цеха);
- времени, отведенного для внедрения GMP.
В любом случае, возможна практика временных защитных мер, которые снизят риски безопасности (компенсируют невыполнение отдельных требований GMP на период устранения несоответствий) и с которыми согласятся аудиторы. Компетентные консалтинговые компании, как правило, могут найти для этого оптимальные решения.
Хотелось бы обратить внимание на еще одну особенность. В большинстве случаев требования аудиторов второй стороны к контрактным производствам базируются на формуле : GMP + СМК . Поэтому в России, где внедрение GMP пока является экзотикой, предприятия, претендующие на конкурентоспособность, должны будут решать эту двойную задачу одновременно. Здесь как нельзя кстати появился в конце 2015 года национальный стандарт: ГОСТ Р 55880–2013 «Продукция парфюмерно-косметическая. Требования к условиям обеспечения безопасности при разработке систем менеджмента качества». Стандарт не имеет европейских аналогов, полностью учитывает все требования ИСО 9001 и ИСО 22 716 (GMP), по сути являясь отраслевой версией ИСО 9001. Комплексное внедрение GMP+СМК будучи, безусловно, оптимальным решением в обеспечении качества и безопасности парфюмерно-косметической продукции, требует, разумеется, определенных усилий. Эти усилия обычно планируют и реализуют в классической последовательности:
- обучение персонала;
- обследование производства и оценка документации;
- планирование работ по устранению несоответствий;
- разработка документации;
- внедрение документации и изменений;
- внутренний аудит, анализ результатов, разработка и проведение корректирующих мероприятий;
- сертификация.
Пункты 1, 2, 4, 5, 6 выполняет, как правило, консалтинговая компания, пункты 3 и 4 – само предприятие, пункт 7 – орган по сертификации.
Многолетний опыт работы авторов в сфере разработки и подтверждения соответствия систем менеджмента позволяет, с учетом специфики GMP и состояния предприятий отрасли, предложить определенную коррекцию этого классического плана.
Во-первых, учитывая характер требований стандарта ИСО 22 716 (строго говоря,- не самого сложного), по нашему мнению, вполне возможно пункты 2, 4 и 6 предприятиям выполнить самостоятельно, имея хорошо обученную рабочую группу (3–5 чел.). Экономия составит до 50% затрат на подготовку. При этом, важнейшим условием, разумеется, является качество обучения. Оптимальным можно считать обучение, которое проводят действующие аудиторы той системы сертификации, в которой предполагается сертификация. Такие обучения проводятся, например, в системах сертификации : «ТЮФ» (Германия), «BSI» (Великобритания), «Системы качества и безопасности пищевой и фармацевтической продукции» (Россия).
Во-вторых, при планировании пункта 7 нужно аккуратно выбирать орган по сертификации. Не секрет, что на российском рынке услуг по сертификации великое множество «самодельных» органов с красивыми названиями и сайтами, «уполномоченных» кем угодно, но не имеющих аттестата Росаккредитации (что, в общем-то является нарушением «Федерального закона о техническом регулировании», который устанавливает, что бумагу вида «сертификат» может выдавать только «аккредитованное лицо»). Проверка простая: запросите у органа по сертификации 6 последних символов из номера его аттестата, войдите на сайт Росаккредитации (fsa.gov.ru), введите их в «поиск» на странице «Реестр аккредитованных лиц» и вы увидите выбранный Вами орган вместе с разрешенной областью деятельности (или не увидите…).
Выводы.
- Выполнение требований технического регламента ТР ТС 009 не является достаточным для внедрения требований GMP на производстве парфюмерно-косметической продукции и соответствия требованиям производителей ведущих зарубежных брэндов для размещения заказов на производство продукции под собственной торговой маркой (СТМ).
- Внедрение требований GMP не требует чрезмерных затрат и может быть проведено в условиях спада производства и финансово-экономического кризиса.
- Оптимальным решением с учетом особенностей российских условий является одновременное внедрение GMP + СМК силами собственного персонала, обученного квалифицированными аудиторами.


